
(좌측부터) 사경하 교수, 정석 교수, 이혜원 교수, 김현호 박사 =자료 고려대학교의료원
고려대학교 공과대학 기계공학부 정석 교수 연구팀이 하버드 의과대학의 김현호 박사, 고려대 의과대학 사경하 교수, 국립암센터 비뇨의학과 이혜원 교수와의 공동연구를 통해 환자의 암세포를 암 주변의 세포와 함께 배양하여 암세포에 대한 항암 약물의 약물 저항성을 확인할 수 있는 미세유체 칩을 개발했고 고려대학교의료원이 최근 밝혔다.
환자 맞춤형 치료를 위해서는 환자 암세포의 유전체 정보 및 암세포의 특성, 암조직의 환경을 고려한 약물 선별이 중요하다. 그러나 종양의 유전적 다양성 때문에 유전체 정보만으로는 적합한 표적 항암제를 제시하기가 어렵다. 쥐를 이용한 동물 실험이 있으나, 그러나 실제 인간의 다양한 세포 및 종양 미세환경을 대변하기가 어려운 케이스도 흔히 보고되고 있다. 이같은 문제를 극복하는 방법은 인간의 세포를 이용하되, 암세포가 자라던 원래 환경의 특성을 재현하는 것이 중요하다고 병원 측은 설명했다.
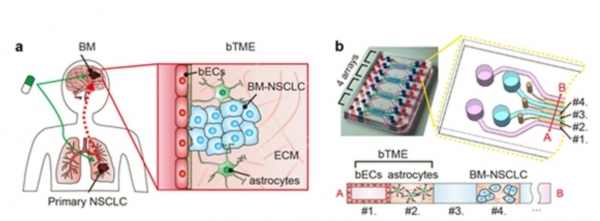
a) 뇌전이성 폐암 환자의 암세포가 자라는 환경에 대한 설명, 암세포, 뇌혈관세포, 성상세포, 세포와 기질 등이 환경을 이루고 있다. b) 뇌로 전이된 세포의 미세환경을 재현하기 위해 본 연구를 통해 개발된 미세유체 칩. =자료 고려대학교의료원
이번 연구는 미세유체 칩 기술을 이용해 암세포 환자에게서 분리한 암세포가 그 주변의 특수한 환경 하에서 자라도록 만들었다고 한다.
연구팀은 특히 뇌로 전이한 폐암을 핵심 타깃으로 개발을 추진했다. 뇌로 전이한 폐암세포는 뇌라는 장기의 특수성으로 인해 기존에 투여되는 약물이 듣지 않는 경우가 빈번하다고 한다. 이는 뇌에만 존재하는 미세환경의 특수성으로, 뇌혈관장벽이나 성상세포들로 인하여 오히려 암세포를 보호하려는 기전이 발생하기 때문이다.
연구진은 뇌혈관 세포, 성상세포, 세포외 기질로 이루어진 미세 환경을 미세유체칩 내에서 배양하여, 뇌 미세환경을 구현하는데 성공했고, 뇌전이 폐암 환자에서 유래된 암세포를 함께 배양하는데 성공했다고 병원 측은 설명했다. 암세포만 배양했을 때와 미세 환경과 공동배양 한 경우의 약물 반응을 유전체 시퀸싱, 분자 단위 프로파일을 이용해 확인한 결과, 뇌의 미세 환경으로 인해 발생하는 폐암세포의 변화가 확인되었다고 연구팀은 설명했다.
기존의 세포 배양 플랫폼과 달리 미세유체 칩은 ▲세포 간의 간격이 micro meter 수준으로 가깝고 ▲미세 유체 채널 내에서 세포들이 분비하는 사이토카인(혹은 화학인자)들의 농도가 빠르게 증가, 유지되기 때문에 세포들 간의 신호 전달이 밀접하게 이루어진다는 특징이 있다. 그리고 이로 인해 암세포와 미세환경 세포들이 실제 환경과 비슷하게 동화되어 가는 과정을 재현할 수 있다고 한다. 연구진은 "기존 항암치료제가 듣지 않는 가장 주요한 원인인 암세포와 주위의 미세환경과의 상호작용을 구현할 수 있는 비임상연구 플랫폼을 개발함으로써 암세포-암주위 미세환경 에코시스템의 분자생물학적 기전 규명 및 이를 타깃으로 하는 새로운 항암치료전략 수립에 활용될 수 있을 것"이라고 밝혔다.
*고려대학교의료원 자료 참고
Copyright © 의약일보










